血糖値を制御するホルモン インスリン:
構造、機能、糖尿病との関係など
UBC/protein_gene/i/insulin
このページの最終更新日: 2026/04/09広告
概要: インスリンとは
インスリン insulin とは、主に膵臓にあるランゲルハンス島の β 細胞で合成されるペプチドホルモンである。GLUT4 というトランスポーター (細胞膜にある輸送体) を介して、細胞内への グルコース の取り込みを促進する。そのため、血糖値を下げる作用がある。
インスリンの重要ポイントは以下の通り。
- インスリンは、食後に膵臓から血液中に放出される。血液中のグルコースやアミノ酸濃度の上昇がインスリンの放出を制御している。
糖尿病 diabetes mellitus は、インスリンの機能不全が原因の病気である。 - ヒトのインスリンは 51 アミノ酸から成り、分子量は 5808 Da (約 6 Ka)。血中濃度は約 50 pM - 250 pM (図、文献 9)。細胞培養で培地にインスリンを添加するときの濃度は、100 nM のオーダーである。

インスリンが代謝に及ぼす影響
インスリンは、上記のグルコース代謝だけでなく、多くの分子の挙動を制御するホルモンである。原則として、食事で得た物質を自分の体に蓄える
一般には
- 解糖を促進
- タンパク質合成を促進
- 脂質合成を促進
と紹介されることが多い。
ここで混乱しやすいのは、「なぜインスリンによって糖は分解されるのに、タンパク質と脂質は合成されるのか?」という点である。
また「インスリンは糖を分解するのに、なぜ同化ホルモンなのか?」という疑問も生じる。
これらの点は、タンパク質と脂質は貯蔵分子 storage molecule であるのに対し、糖はそうでない (immediate energy である) と考えると理解しやすい。つまり「糖・タンパク質・脂質」は対応関係になく、貯蔵型の糖であるグリコーゲンをもってきて「グリコーゲン・タンパク質・脂質」として考えなければならない。
つまり、インスリンは糖・アミノ酸・脂質の貯蔵分子に対して
- グリコーゲン合成を促進
- タンパク質合成を促進
- 脂質合成を促進
という作用を示す。さらに、貯蔵分子の各構成要素に対して
- 糖の細胞への取り込みと解糖 (グリコーゲンの材料である G6P および脂質の材料であるアセチル CoA の生成) を促進
- 遊離アミノ酸の細胞への取り込みを促進 (糖と異なり、タンパク質合成に際してアミノ酸は分解される必要がない)
- アセチル CoA の合成 (すなわち解糖および遊離アミノ酸の分解) を促進
という作用を示すと考えると、インスリンが栄養素の代謝に及ぼす影響を統合的に理解することができるだろう。
| 食欲制御 |
この意味で、「脳 ではインスリンは異化ホルモンである」という言い方がされることもある。 |
| 脂質 の同化 |
インスリンは 脂肪酸合成 を促進する。
|
| 脂質 の異化 |
飢餓によって、ピルビン酸からアセチル CoA への変換を行う PDK4 が阻害される。ピルビン酸は基本的に糖代謝の産物なので、これはエネルギー源が糖質から脂質へシフトすることを意味する。これもインスリンの作用なのか (インスリンが PDK4 を活性化しているのか)、要確認。 |
| 糖質 の同化 |
インスリンは解糖を促進する。これは異化作用であるが、グルコースから生じた G6P がグリコーゲン合成に使われたり、 アセチル CoA が脂肪酸合成に使われたりする場合は同化作用と言える。つまり、グルコースの分解自体は同化かつ異化 (またはどちらとも言えない) である。 インスリンは細胞への糖取り込みを促進する。
インスリンは解糖を促進する。詳細は各酵素のページを参照。 インスリンは グリコーゲン 合成を促進する。
|
| 糖質 の異化 |
インスリンは 糖新生 を抑制する。
インスリンはピルビン酸の完全な酸化を阻害するため、インスリン存在下ではグルコースの多くが乳酸になる (8)。 |
タンパク質の同化 |
インスリンは タンパク質 の同化を促進する。
|
タンパク質の異化 |
インスリンはオートファジーおよびプロテアソーム依存的なタンパク質分解を抑制する。 |
広告
「あとがき」で当サイトを参考にしたと書いてくれているラノベです。Kindle Unlimited で読めました。ストーリーと文章が良く、面白かったです。
インスリンの構造
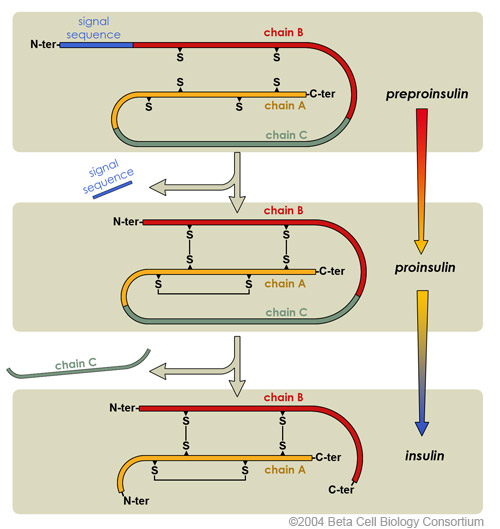
インスリンは、ひと続きのポリペプチドである preproinsulin として翻訳され、プロテアーゼによる消化を受けて活性型になる。活性型のインスリンは、ジスルフィド結合で繋がった 2 本のポリペプチドである。概要は以下の図に示されている (3)。
- シグナルペプチドの除去
- 特徴的な 3 つのジスルフィド結合の形成
- C ペプチドの除去
が主要なステップである。
なお、インスリンに構造が類似したペプチドホルモン、インスリン様成長因子 (insulin-like growth factor; IGF) では C ペプチドが除去されず、活性型 IGF は 1 本のポリペプチドである。
似たような図をいくつか置いておく。クリック拡大できる。

|
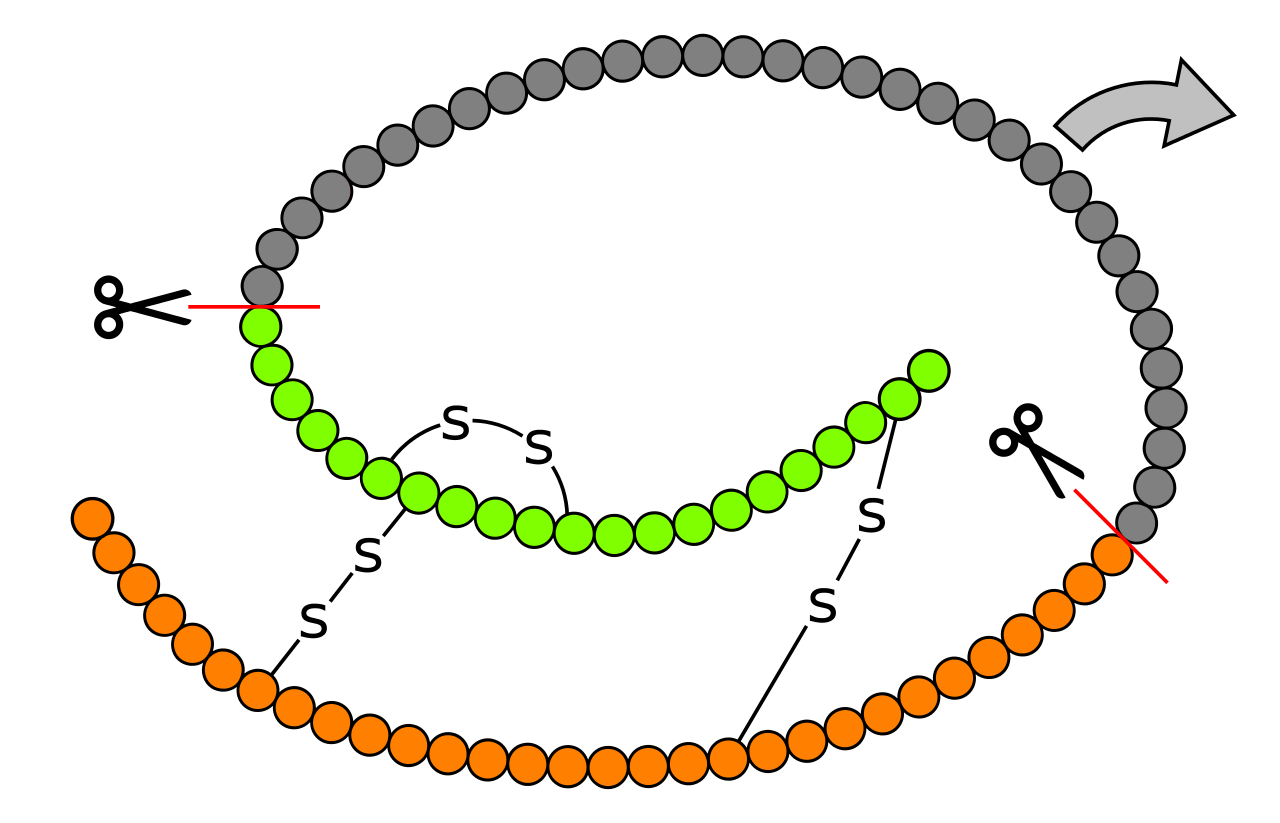
|
インスリンの合成と分泌
グルコースを食事として摂取する方が、注射するよりもインスリン分泌を促進する。血糖値だけでなく、腸管からのシグナルがインスリンの合成・分泌に重要である。
インスリンシグナル
更新予定。とりあえずは関連ページを参照のこと。
>「鳥への進化はインスリン耐性から始まった」というプレスリリースがあった (8)。
- インスリンが受容体に結合してもシグナル伝達が起こらない。インスリンはピルビン酸の完全酸化を阻害するため、結果として酸化的リン酸化が促進され、多くのエネルギーが得られる。
- インスリンシグナルの抑制は老化抑制にも繋がっている。一般に、鳥は哺乳類よりも長寿である。
糖尿病治療薬としてのインスリン
糖尿病は、部分的なインスリンの不足 (量的な不足、またはインスリン抵抗性による機能的な不足) によって血糖値が高く保たれる病気である。このサイトにも関連ページが多数あるので、興味がある人は検索してみてほしい。

食事および運動療法が糖尿病治療の基本であるが、3 ヶ月以上行っても HbA1c が 6.5% 以上の場合、
インスリン製剤は、作用の発現時間および持続時間により、以下のように分類される (4)。
超速効型 |
皮下注射後 10 分以内に効果が現れる (4)。食事直前に皮下注射する。超速効型および速効型は、インスリンが完全に溶解しているので、見た目が透明である。 |
速効型 |
皮下注射、点滴などさまざまな使用法がある (4)。皮下注射の場合は、食後の血糖値上昇を抑えるため、食事 30 分前に使われる。 |
混合型 |
速効型と中間型の混合製剤 (4)。それぞれの割合によって、複数の種類がある。 |
中間型 |
文献 4 では特徴が書かれていない。 |
持続型 |
中間型よりも持続時間が長い。インスリンの基礎分泌を補う目的で使われる (4)。。 |
また、インスリン製剤はその由来によって以下のように分類される。
ヒトインスリン製剤 |
ヒトのインスリン。 |
インスリンアナログ製剤 |
インスリンの構造に手を加えることで、その薬物動態を改善したもの。 |
インスリン製剤は 1920 年代に使われるようになり、当時のものは ウシ や ブタ の膵臓から精製されていた (5)。
広告
References
Volkow et al. 2011a (Review). Reward, dopamine and the control of food intake: implications for obesity. Trends Cogn Sci 15, 37-46.- Amazon link: ストライヤー生化学
: 使っているのは英語の 6 版ですが、日本語の 7 版を紹介しています。参考書のページ にレビューがあります。
Witters et al. 1988a. Insulin stimulates the dephosphorylation and activation of acetyl-CoA carboxylase. PNAS 85, 5473-5477.- Amazon link: ナースのためのくすりの事典 2017年版
: 使っているのは 2007 年版ですが 2017 年版を紹介しています。
- 糖尿病アカデミー 進化する注射薬. Link: Last access 2019/02/08.
- By Uploaded by Fred the Oyster, CC BY-SA 4.0, https://commons.wikimedia.org/w/index.php?curid=35286441
- By Proinsulin.gif: Original uploader was Mr Hyde at cs.wikipediaderivative work: Zapyon (talk) This W3C-unspecified vector image was created with Inkscape . - Proinsulin.gif, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=16891004
Satoh 2021. Bird evolution by insulin resistance. Trends Endocrinol Metab 32, 803-813.- By Mcstrother - Own work, CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=15758660
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。