ゲノム編集技術の概要: CRISPR, ZFN, TALEN など
UBC/experiments/dna/genome_modification
このページの最終更新日: 2026/04/09広告
概要
変異動物の表現型から原因遺伝子を探す遺伝学をフォワードジェネティクス forward genetics という。一方、遺伝子に変異を導入し、その表現型から遺伝子の機能を調べる方法をリバースジェネティクス reverse genetics という (図, Ref. 4)。
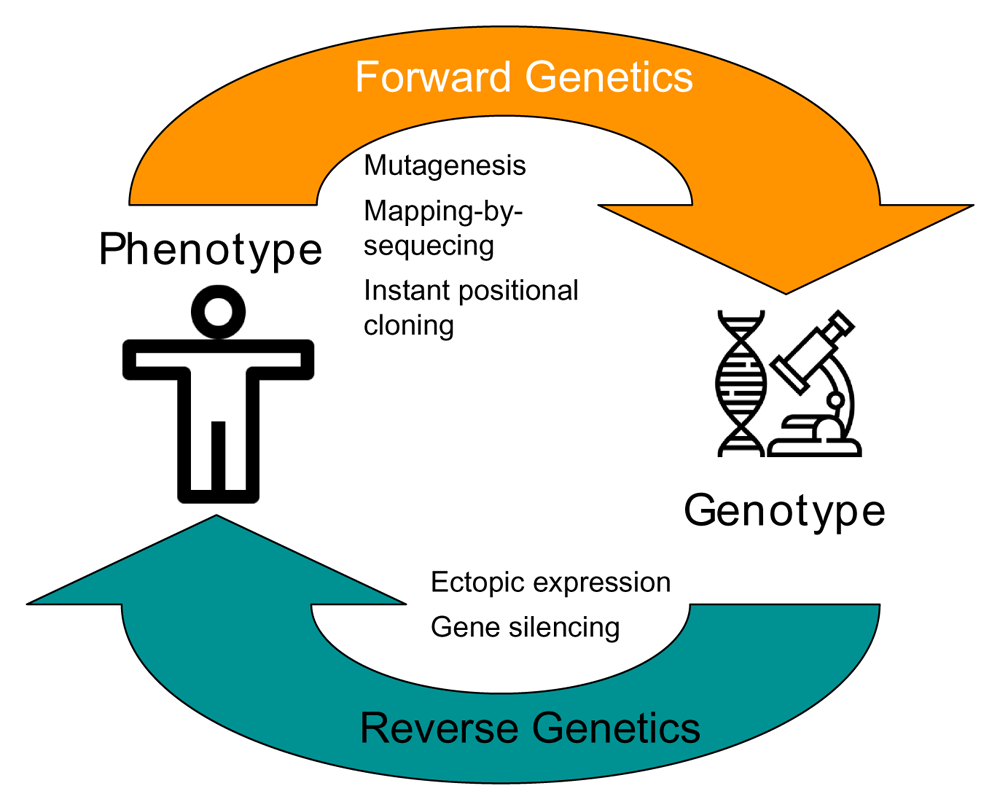
ゲノム編集技術は、リバースジェネティクスに不可欠な技術である。
> ゲノム編集技術は、次のような流れで成立してきた (1)。
- 1970 年代に、トランスジェニック動物が作られるようになった。
- 1980 年代 ES 細胞が樹立。80 年代後半には ES を用いた遺伝子改変動物が作られた。
- 2000 年にヒトゲノム、2002 年にマウスゲノムが解読。
- 2007 年 ES 細胞を用いた遺伝子改変技術に ノーベル医学・生理学賞。
ゲノム編集の基本的な考え方は、以下のいずれかである。
- 相同組み換えを利用する。
- DNA の二本鎖を切断し、修復時に改変する。
相同組み換え
歴史的には、
ただし、バクテリアなどの微生物では効率の低さを数でカバーできるので、相同組み換えによるゲノム編集は未だに有効な手段である。大腸菌に関する文献 6 から少しメモしておく。記述そのままではなく、新しい方法も加えている。
遺伝子ノックアウトを例にとる。ごく簡単に述べると、以下のような原理である。ベクターを直鎖状にして導入するため、linear transformation と呼ばれる。元文献は Winans et al., 1985。
- 両側のゲノム配列それぞれ 500 bp 程度を加えて、目的遺伝子 (潰したい遺伝子) をベクターにクローニングする。目的遺伝子の 5' 側 500 bp + 薬剤耐性遺伝子 + 目的遺伝子の 3' 側 500 bp で in-fusion すれば一発で作れるはず。かつてはベクター上の目的遺伝子を薬剤耐性遺伝子に入れ替えていたようだが、どうやっていたのかよくわからない。
- 次に、ベクターを制限酵素などで直鎖状にして、大腸菌 recD 株に導入する。必要なのは薬剤耐性遺伝子とその両側の 500 bp ずつだが、他の部分があっても問題ないことが多い。recD はエキソヌクレアーゼである RecBCD をコードする遺伝子の一つで、これで薬剤耐性遺伝子が大腸菌のゲノムに導入される。
- これを選択培地に撒いて、生えてきたコロニーが遺伝子欠損株である。念のため PCR などで確認することが多い。
- この方法だと、ノックアウトできる株が recD 株に限定される。たとえばタンパク質発現のときは BL21 株などがよく使われるが、望みの株でノックアウトできないのが欠点。P1 transition によって自分の株にゲノムを移す必要がある。
DNA 切断による遺伝子編集法
相同組み換えの他に TALEN や ZFN といったゲノム編集技術が知られていたが、これらの方法ではタンパク質 protein が標的配列を認識するため、標的ごとに protein engineering が必要であった (4)。一方、CRISPR/Cas9 では
図は Ref. 5 より。
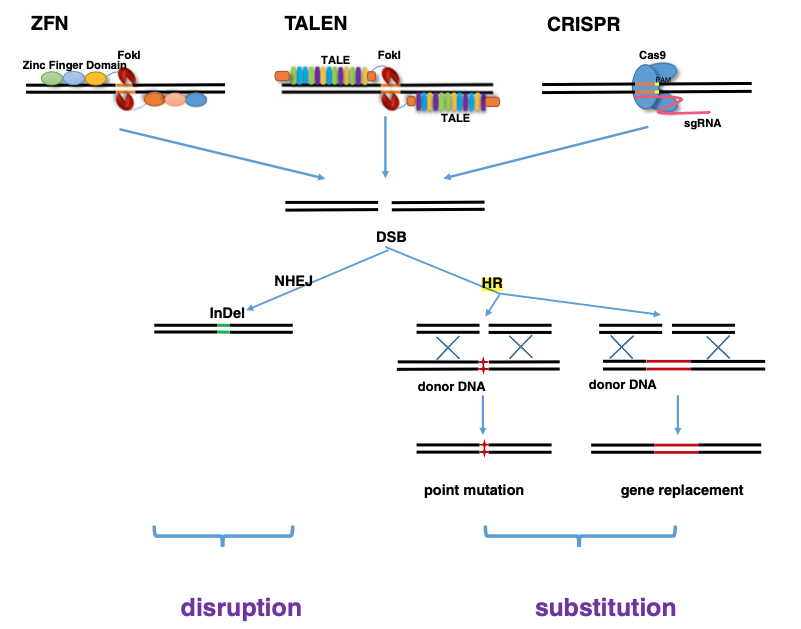
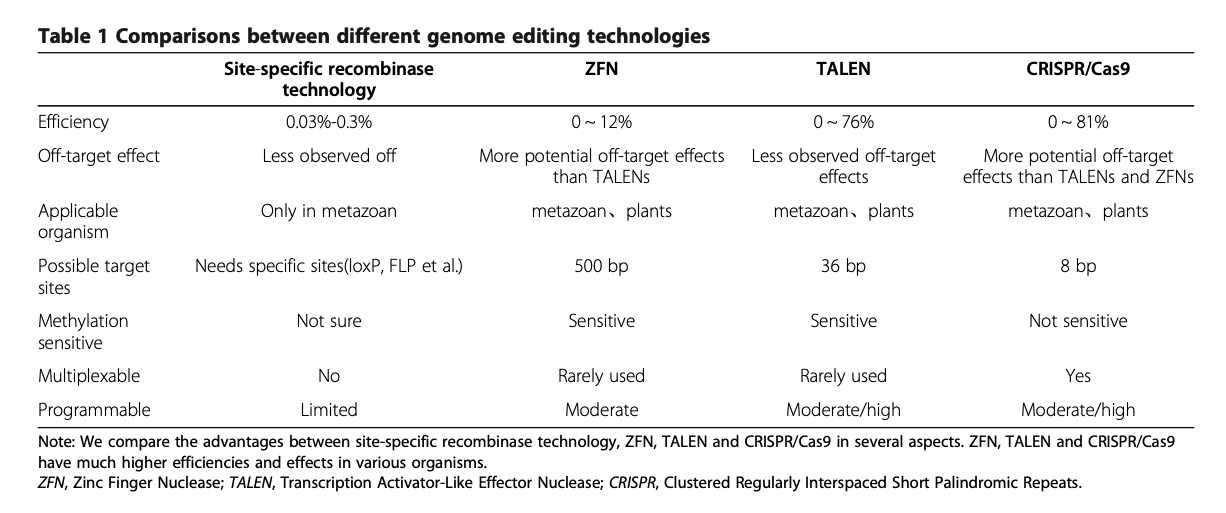 広告
広告References
河合, 2016a. ゲノム編集技術の現状と可能性. J Anim Genet 44, 23–34.Pellagatti et al. 2015a (Review). Application of CRISPR/Cas9 genome editing to the study and treatment of disease. Arch Toxicol 89, 1023-1034.Hsu 2014a (Review). Development and applications of CRISPR-Cas9 for genome engineerging. Cell 157, 1262-1278.- Khan AA, Raess M and de Angelis MH. Moving forward with forward genetics: A summary of the INFRAFRONTIER Forward Genetics Panel Discussion [version 1; peer review: 1 approved, 1 approved with reservations]. F1000Research 2021, 10:456 https://doi.org/10.12688/f1000research.25369.1
Chen et al. 2014b. Advances in genome editing technology and its promising application in evolutionary and ecological studies. GigaScience 3, 24.山田 2003a. バクテリアにおける遺伝子破壊株の作製方法. Environ Mutagen Res 25. 87-92. Pdf link: Last access 2024/12/11.
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。
