コンピテントセルの作り方、保存方法
UBC/experiments/dna/competent_cell
このページの最終更新日: 2026/04/09広告
概要: コンピテントセルとは
プラスミドを細胞に導入することを形質転換 transformation といい、薬品で処理することによってプラスミドを取り込みやすくなった細胞をコンピテントセル competent cell という。
このページでは、大腸菌コンピテントセルの作成方法をまとめる。形質転換の手順については、transformation のページ を参照のこと。
原理
コンピテントセル作成の原理は、塩またはその他の薬品で
細胞膜のリン脂質部分およびプラスミドは、ともに負電荷をもっている。したがって、大腸菌培養液にプラスミドを加えても、両者は十分に近づかない (画像は Public domain)。
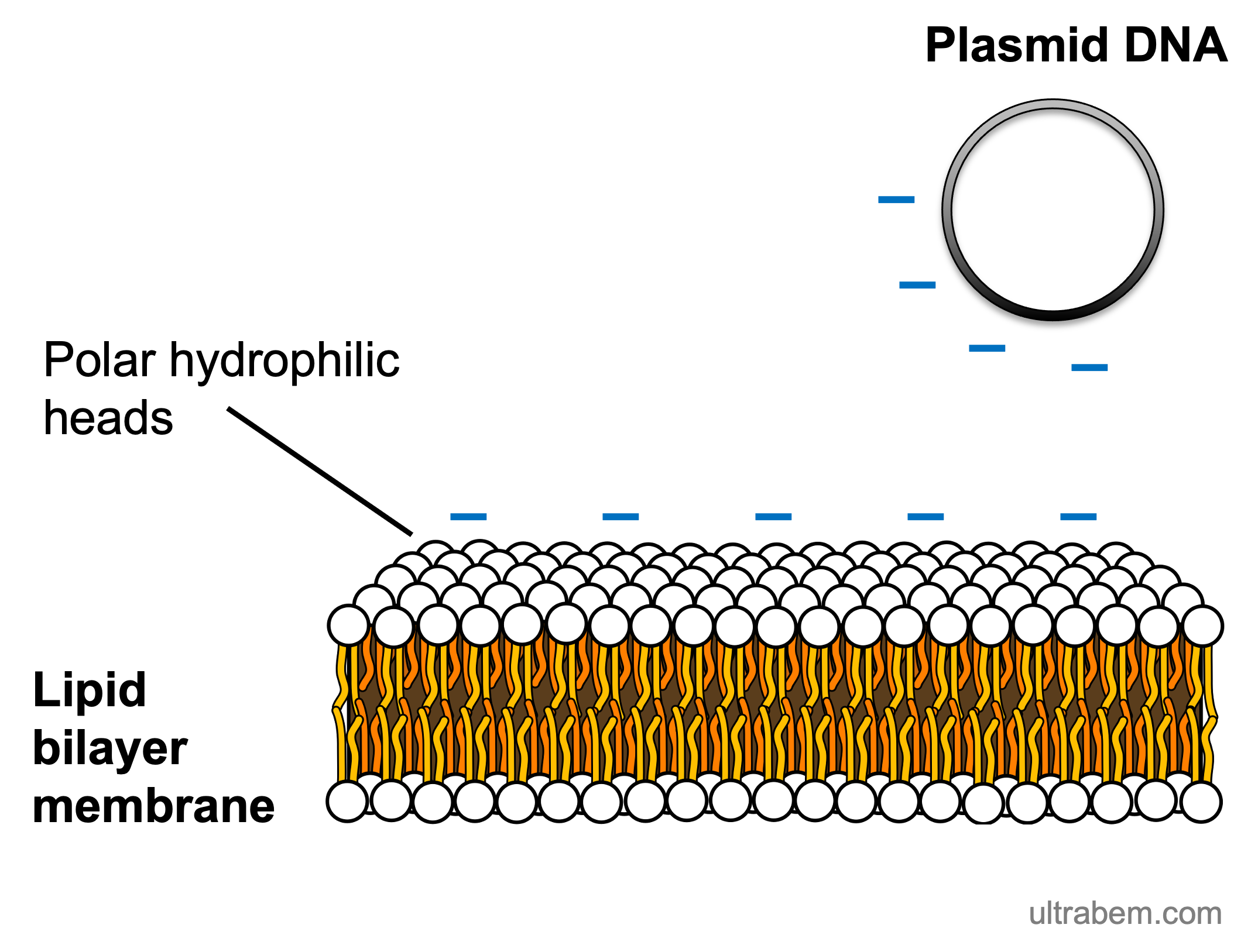
コンピテントセル作成では、大腸菌を塩溶液で処理する。マグネシウム塩やカルシウム塩がよく用いられる。これらの陽イオンが細胞膜およびプラスミドの負電荷を中和する。
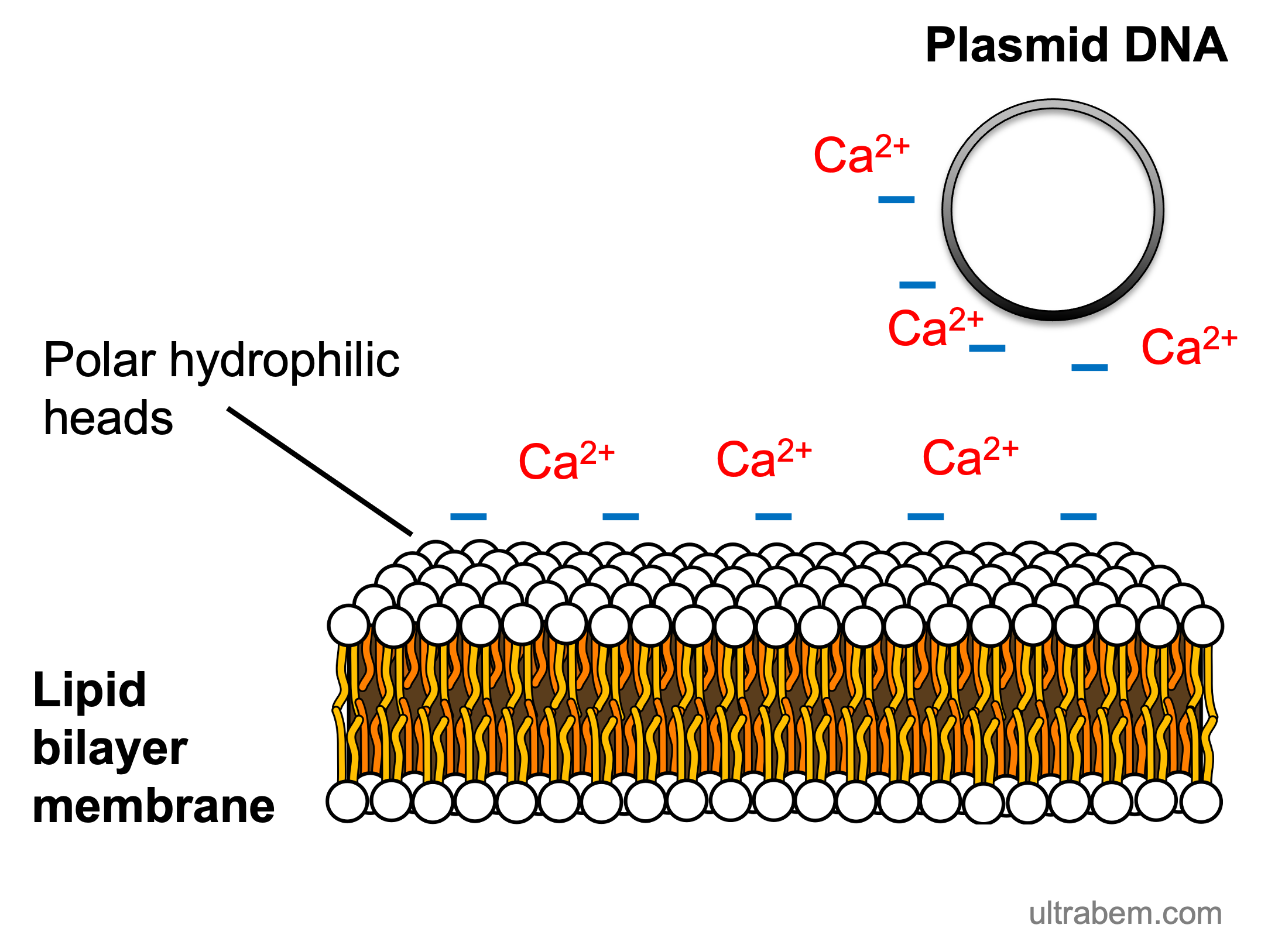
これによって、プラスミドと大腸菌が十分に近づくことができるようになり、ヒートショックやエレクトロポレーションによる形質転換が可能になる。
以下のような試薬が、コンピテントセル作製によく使われる (2)。
| CaCl2 | 負電荷を中和する。 |
| MgCl2 | CaCl2 と同様に働くが、DNA がより多く細胞膜に結合するようになるらしい。 |
| RbCl | CaCl2、MgCl2 と同様に働く。より高いコンピテンシーが得られるようだ。 |
| DMSO | リン脂質部分を集合させ、膜の透過性を上げる。 |
| PEG | DNA およびリン脂質の負電荷をブロックする。 |
推奨プロトコール
コンピテントセル作製のプロトコールはたくさんあるが、以下の方法がシンプルで好きである (1)。
- DH10, DH-5α などのコロニーをピックアップし、6 mL の LB 培地 で 37°C で振盪しながら終夜培養する。
- この培養液を 300 mL の LB に加え、550 nm の吸光度が 0.45 - 0.55 になるまで培養する。37°C で約 2 時間。
- 50 mL チューブ中、2,500 rpm, 15 min 遠心する。以降の作業は全て氷冷下で行う。
- 上清を完全に除き、15 mL 氷冷 0.1 M MgCl2 に大腸菌を懸濁。
- 2,500 rpm, 15 min で遠心、上清を除き 20 mL 氷冷 0.1 M CaCl2 に懸濁。
- 氷上で 20 min 静置し、2,500 rpm, 10 min 遠心。
- 上清を完全に除き、6 mL の 0.1 M CaCl2/15% グリセロール に再懸濁。
- 100 µL ずつに分注し、-80°C で保存する。
2 番のところでは、色々なバリエーションがある。まず、上のプロトコールでは 6 mL の前培養液を 300 mL に加えるので、これは 2% と表現される。前培養液の添加量は、1 - 2% が標準的である。
2 番の培養温度も重要である。上のプロトコールでは 37°C だが、ここは低温の方が良いという場合もあり、30 °C で培養するケース、18 °C で培養するケースなど様々である。低温での培養時間は、液量に左右される。フラスコに余裕があるほど、振盪によって酸素が供給されるので、増殖は早くなる。経験上、50 mL フラスコに 5 mL の培地を入れて激しく振盪すると、1% 前培養液、18 °C でも 4 - 5 時間程度で使用可能な OD に達する。
注意事項など
0.1 M 塩化マグネシウムで大腸菌を懸濁するステップで、間違って 1 M のストック溶液を使ってしまったことがあったが問題なし。大腸菌は高塩濃度に強いのかもしれない。
保存は -80°C である。グリセロール溶液中に保存するので、グリセロールストックの作り方 のページにあるように、-20°C保存とも思われるが、おそらく温度が高いと徐々にコンピテンシーが失われていくのだろう。
その他のプロトコール
その他のプロトコールについては詳述せずに、特徴を表にまとめる。
| リンク | メモ |
|---|---|
| 三重大学 |
References
- Preparation of competent E. coli cells using calcium chroride. Cocoa Biotech. Last access 2017/07/15. リンク切れ 2023/02/18. http://www.koko.gov.my/CocoaBioTech/DNA%20cells23.html
- Introduction to Competent Cells. Link: Last access 2023/02/18.
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。
