PI3 キナーゼ: 分類、構造、機能など
UBC/protein_gene/p/pi3k
このページの最終更新日: 2026/04/09- 概要: PI3K とは
- PI3K の分類
- PI3K の構造
- 調節サブユニット p85
- 触媒サブユニット p110
- PI3K の機能
広告
概要: PI3K とは
PI3K は phosphoinositide 3-kinase または phosphatidylinositol 3-kinase の略で、イノシトールリン脂質のイノシトール環 3 位のヒドロキシル基 (-OH) をリン酸化する酵素である。
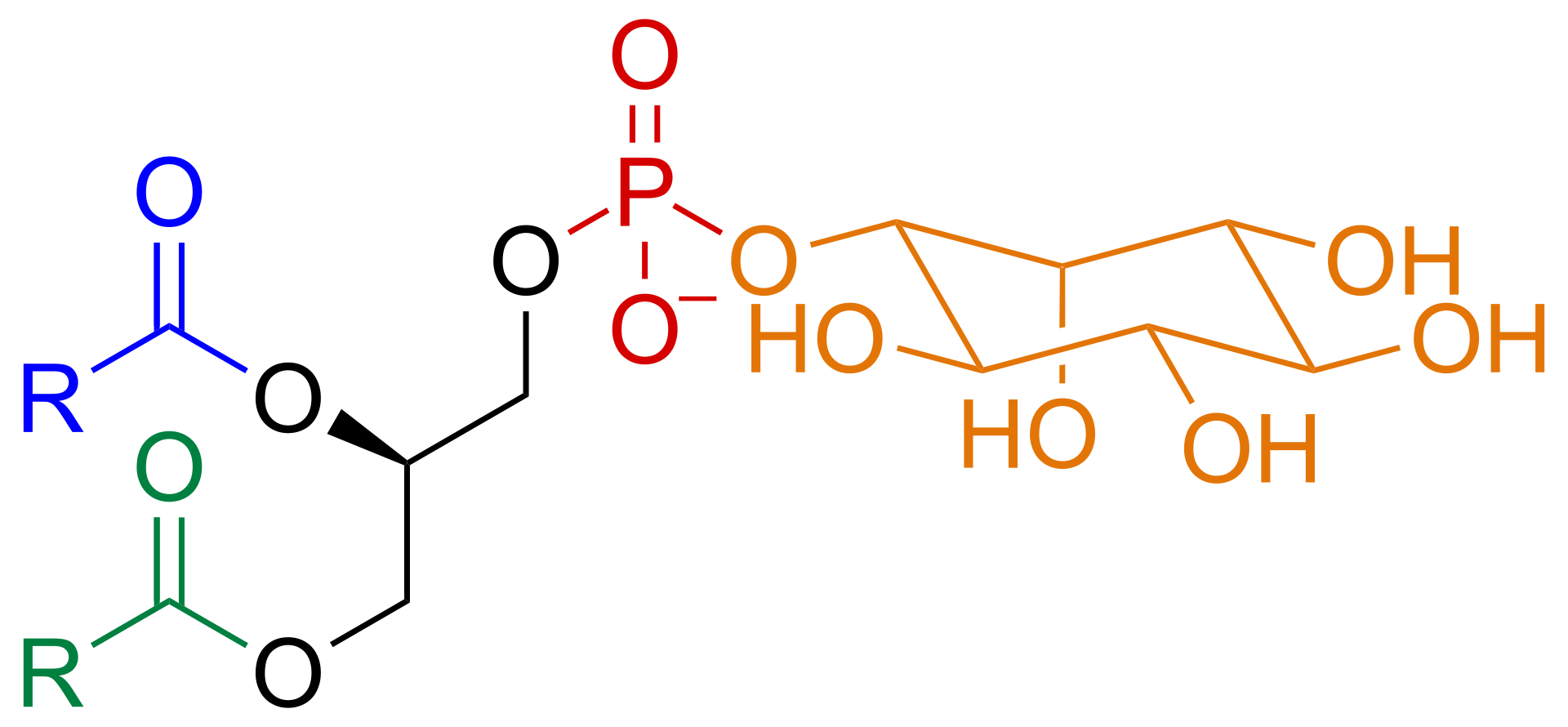
図 (Ref 4) はホスファチジルイノシトールの構造で、右にあるオレンジで示された六員環がイノシトール環である。
イノシトール環の炭素番号は グリセロール 部分と繋がっている部分が 1 番であり、そこから図のように番号がついている (7)。かなりわかりにくいが、1, 2, 3 および 5 番は環から下方へ、4 および 6 番は上方へそれぞれ官能基がついている。イノシトール のページも参照のこと。
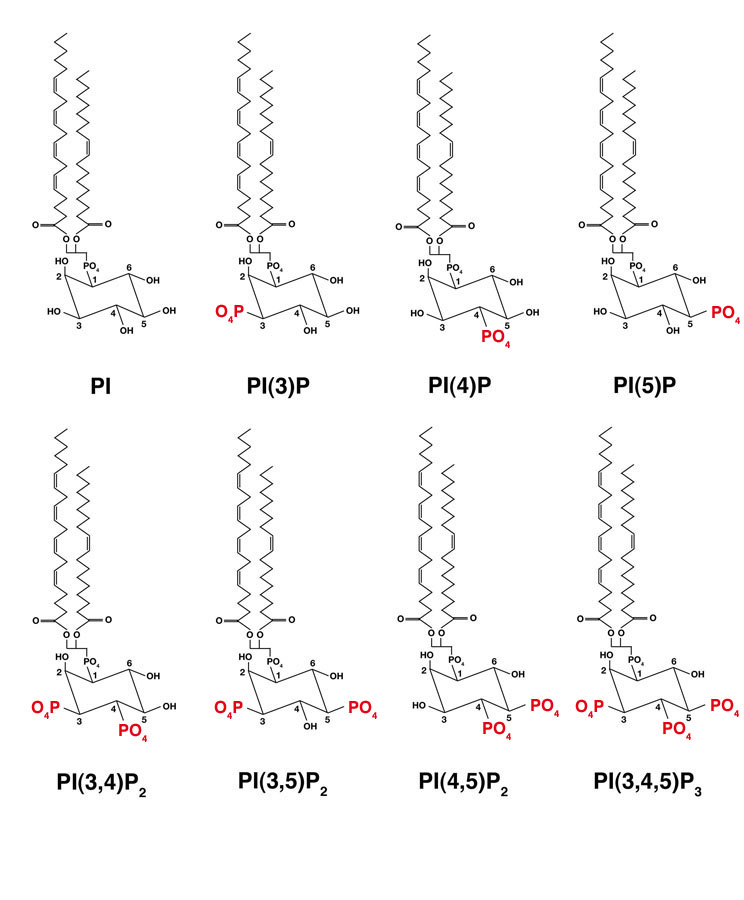
PI3K には I - III 型のファミリーが存在する。Class I はヘテロ二量体であり、調節サブユニットと触媒サブユニットがある。Class II および III には調節サブユニットはなく、単量体で活性を示す。
Class I PI3K は、アミノ酸配列の相同性から、さらに Class IA および Class IB に分類される。
Class I |
複数の遺伝子がある。以下はヒトの遺伝子。 PI3KR1: 選択的スプライシングにより、p85α、p55α、p50α の 3 種類のタンパクをコードする。 PI3KR2: p85β をコードする。 PI3KR3: p85γ をコードする。 |
Class I |
p110α、p110β および p110δ があり、それぞれ PI3KCA, PI3KCB, PI3KCD という遺伝子にコードされる。 PI3KCG という遺伝子にコードされる p110γ は Class IB PI3K に分類され、主に 血液 細胞で発現する。 |
Class II |
p110 に似た単量体から成る。 |
Class III |
酵母の vacuolar protein sorting 34 (Vps34) など。Ras-binding domain を欠く。 |
広告
「あとがき」で当サイトを参考にしたと書いてくれているラノベです。Kindle Unlimited で読めました。ストーリーと文章が良く、面白かったです。
PI3K の構造
以下は、Class I から III の PI3K 構造の模式図である (7)。単量体で機能する Class II および III は、kinase domain (図の KD) が必要であることからも推察されるように、Class I PI3K p110 サブユニットに似ている。
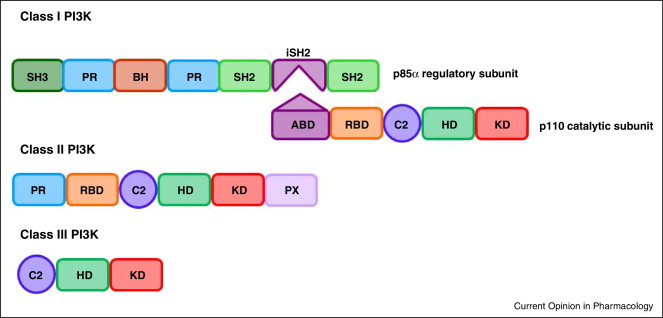
Figure 1. Schematic representation of class I-III PI3K structures ABD: adaptor binding domain; RBD: RAS binding domain; C2: C2 domain; HD: helical domain; KD: kinase domain; PR: proline rich domain; PX: phox homology domain; BH: breakpoint cluster region homology domain (Rho-Gap-like domain); iSH2: inter-SH2 domain (p110 binding domain). Complexes between p110α, p110β, p110δ and p110γ and their respective regulatory subunits are often referred to as PI3Kα, PI3Kβ, PI3Kδ and PI3Kγ.
調節サブユニット p85
調節サブユニット p85 には以下のようなドメインがある。
SH3 domain |
|
Pro-rich domain |
|
BH domain |
Bcr homology domain の略で、 |
SH2 domain |
|
iSH2 domain |
p85 の 2つの SH2 domain 間の配列 (IS2; inter-SH2 domain) で、ここで p110 の p85 結合ドメインと結合する。 |
> C. elegansのP85 subunitに相当するAAP-1 に関する論文 (2)。
- p85, p55, p50alpha, p85betaは全てYXXM motifに結合。p110をリクルートし活性化する。
- SH2 domainが2つ並んでいる分子をデータベースで検索。AGE-1 adaptor protein (aap) と名付けた。
- AAP1とAGE-1の結合を確認した。
- マウスでは、p50/p55α は、p85α の insulin-stimulated p110 活性化を補償できる。
- aap-1 mutant phenotype が微妙なので、通常のシグナルに必須ではないと考えられる。dauer arrest mutant のスクリーニングにも引っかかってこなかった。
- Drosophila の Dp60 null mutant は p110 のそれよりも表現型が弱い。Regulatory subunitは重要でない。
触媒サブユニット p110
p85結合ドメイン - ras結合ドメイン - C2 domain - PIKa (PI 3-kinase family, accessory) domain - kinase domain.
ras結合ドメインにはrasが結合し、PI3K活性を制御する。C2 domainは、一般にCa2+依存的、あるいは非依存的に膜リン脂質と結合する。PIKa domainの役割は不明である。
p70S6K、some isoforms of PKC、Akt/PKB (3)。
p110alpha, beta, deltaの3種が存在。alpha, betaは広範な組織で発現するが、deltaは白血球のみ。
- LY294002 で insulin-stimulated glucose transort と GLUT4 translocation が両方止まる (1)。
- PDGF でも PI3K は活性化されるが、糖取り込みは起こらない。
- 3T3-L1 を用いた解析から、p110beta が糖取り込みに重要とされてきた。
- Rac, CdC42 などは PIP3 が集まっている場所で活性化し、アクチン重合を引き起こすことが知られている。
広告
References
Clark et al. 1998a. Intracellular localization of phosphatidylinositide 3-kinase and insulin receptor substrate-1 in adipocytes: potential involvement of a membrane skeleton. J Cell Biol, 140, 1211-1225.Wolkow et al. 2002a. Insulin receptor substrate and p55 orthologous adaptor proteins function in the Chaenorhabditis elegans daf-2/insulin-like signaling pathway. JBC, 277, 49591-49597.Tsakiridis et al. 1996. Insulin activates a p21-activated kinase in muscle cells via phosphatidylinositol 3-kinase. JBC, 271, 19664-19667.- By Hbf878 - Own work, CC0, Link
- By Kiyok - 本人作成 (Self-made), Public Domain, Link
- ホスファチジルイノシトール, 脳科学辞典. Link: Last access 2019/06/19. CC-BY.
Stark et al. 2015a. PI3K inhibitors in inflammation, autoimmunity and cancer. Curr Opin Pharmacol 23, 82-91.
Stark et al. (2015a) is an open-access article distributed under the terms of the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited. Also see 学術雑誌の著作権に対する姿勢.
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。
