ヘイフリック限界と細胞の老化:
定義、がん細胞との関係など
UBC/cell/cell_cycle/hayflick_limit
メタ目次 老化 にも分類されています
- 概要: ヘイフリック限界とは
- ヘイフリック限界とテロメア仮説
- ヘイフリック限界と個体の寿命
- 細胞老化に伴う分子レベルの変化
広告
概要: ヘイフリック限界とは
ヒトの細胞を培養した際、分裂可能な回数が決まっている。この回数を
ヘイフリック限界は、Hayflick and Moorhead によって 1961 年に報告された (2)。ヒトの線維芽細胞が使われたようである。この報告は、以下に述べるような意義をもっていた。
- 1961 年当時、人々は細胞の分裂回数は基本的に無限であると考えていた (1)。
- 時間経過による 老化 chronological aging ではなく、分裂回数による老化 replicative senescence という概念をもたらした。
- 細胞内に分裂回数をカウントする道具があることを示唆し、のちのテロメアおよび テロメラーゼ の発見に貢献した。
ヘイフリック限界とテロメア仮説
ヘイフリック限界のメカニズムは、基本的にテロメアであると考えて良さそうである (図, ref. 3)。
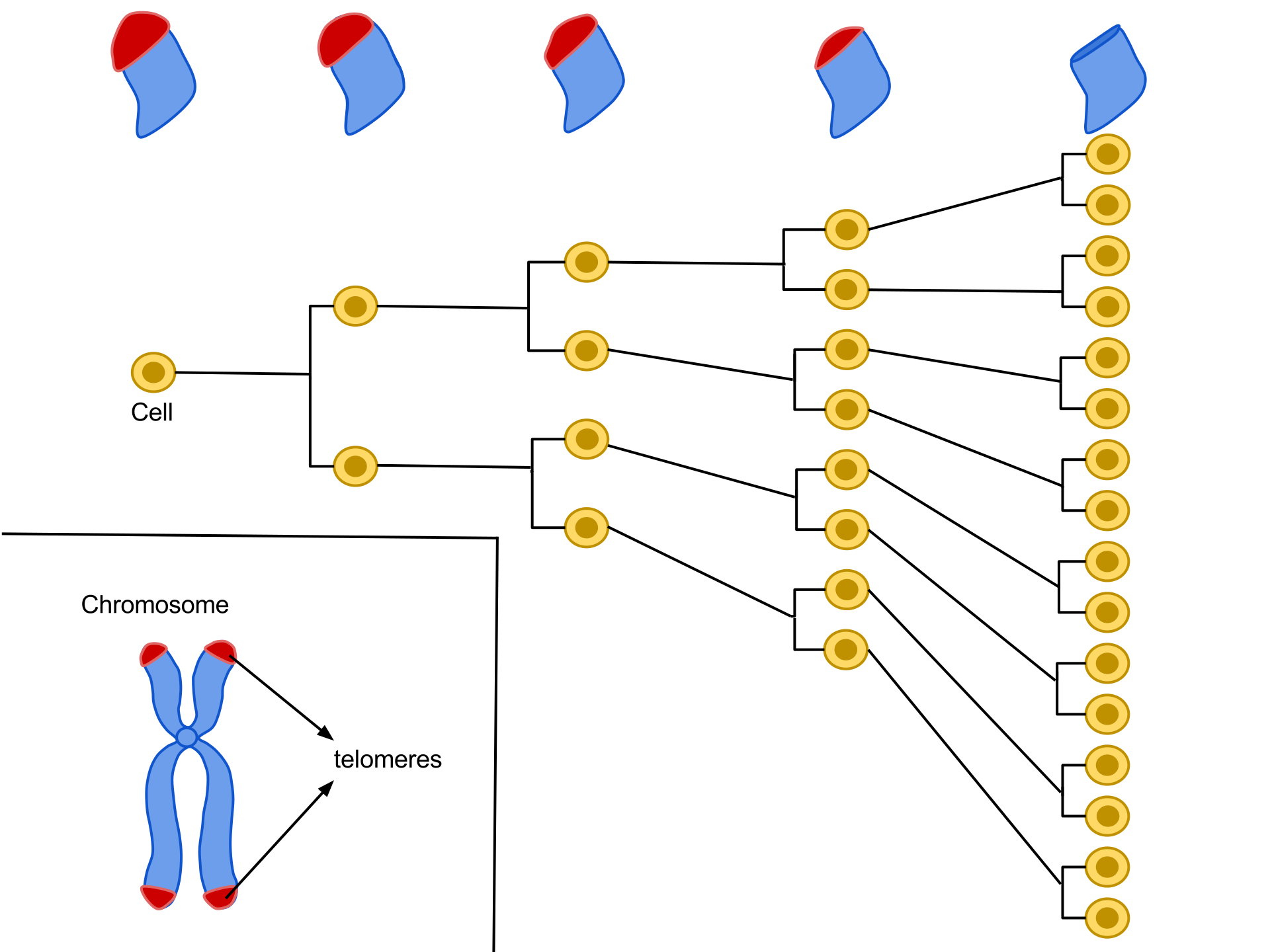
つまり、細胞分裂 のたびに染色体末端にあるテロメアが短くなる。この領域は DNA の複製に重要であり、短いと分裂が阻害される。
そのため、動物はテロメアを伸長する酵素テロメラーゼをもっているが、この活性はほとんどの細胞において発生過程で失われる (4)。ゆえに、体細胞は有限回数しか分裂できない。これがテロメア仮説である。
なお、生殖細胞、幹細胞および がん の細胞にはヘイフリック限界がない。これらの細胞はテロメラーゼが発現している。ほとんどのがん細胞では、テロメラーゼが発現するような変異が入っていることが知られている。
> テロメア仮説の解説 (4)。
- 生殖細胞テロメアは 15 kb 程度で、これが分裂のたびに短くなる。
- 5 - 7 kb 程度でヘイフリック限界に達する (この論文では M1 と呼んでいる)。
- 通常はそこで分裂を停止するが、何らかの原因で分裂が継続すると、2 - 4 kb 程度で
M2 crisis に達する。ここでは、染色体の構造が不安定になるため、細胞死が起こる。
p53 や Rb に異常があると、細胞老化が起こらず M2 クライシスを起こす (Ref)。クライシスの状態ではテロメアが融合しており、集団のほとんどの細胞が死滅する。生き残った細胞は腫瘍化する可能性がある。
広告
「あとがき」で当サイトを参考にしたと書いてくれているラノベです。Kindle Unlimited で読めました。ストーリーと文章が良く、面白かったです。
ヘイフリック限界と個体の寿命
細胞老化 (= 分裂の停止) は、個体の老化を一部しか説明しない。
- 個体の老化は連続的なプロセスであるが、細胞老化は「細胞周期の停止」として定義できる連続的でない現象なので、両者は相いれない (4)。ただし、多くの細胞が少しずつ分裂を停止すると考えれば解釈は可能。
- 多くの組織で、細胞分裂がずっと起こっているわけではない (4)。造血系、免疫系などでは分裂が重要だが、神経系では分裂は基本的に停止している。
細胞老化に伴う分子レベルの変化
まず、老化した細胞では細胞周期がストップし、細胞は G1 phase に留まる (5)。このとき p21 や p16 などの cell cycle inhibitor の発現が増大している。
また、老化した細胞ではクロマチン構造の変化が起こる (6)。ゲノムのメチル化は全体的に減少するが、一部の領域ではメチル化が増える。ヒストン も脱アセチル化が進み、senescence-associated heterochromatin foci (SAHF) と呼ばれる特殊な領域を作り出す。クロマチン構造の変化は、細胞周期を進めるような遺伝子の発現抑制に繋がっていると考えられている。
> pH 6 の β-ガラクトシダーゼ活性が細胞老化のマーカーになるという論文 (7)。
- β-galactosidase 活性は多くの酵素の活性の和であり、老化のマーカーになるのは主としてリソソーム由来の β-ガラクトシダーゼ活性である。
- 活性が上がるという報告はかねてからあり、12 の細胞株を 1 年 (passage ~80) 培養して再現性をチェックしている。
- 結果は positive で、確かに実際の培養日数よりも、分裂回数によって増加していた。
- 細胞を染色し、positive cell の割合でデータをとっている。
広告
References
Shay and Wright 2011a (Review). Role of telomeres and telomerase in cancer. Semin Cancer Biol 21, 349-353.Hayflick and Moorhead 1961a. The serial cultivation of human diploid cell strains. Exp Cell Res 25, 585–662.- By Azmistowski17 - Own work, CC BY-SA 4.0, Link
Morin 1997a (Review). Telomere control of replicative lifespan. Exp Gerontol, 32, 375-382.Kirkwood 1999a. 生命の持ち時間は決まっているのか - 「使い捨ての体」理論が開く希望の地平.
|
生命を germ line と soma に分け、寿命を説明しようとする使い捨ての体理論 disposable soma theory に関する本。Kirkwood は多くの論文や総説を発表している一流の老化研究者でもある。 Germ line とは生殖細胞系列のことで、次の世代に伝える遺伝情報がこれらの細胞に保持されている。そのため、germ line cell には生物は多大なエネルギーを投資し、DNA が傷ついたりしないように配慮している。 一方、それ以外の体細胞 soma には不必要なエネルギーを投資しない。これらが古くなってきたら、新しい体に作り変えれば良いためである (繁殖活動)。Pierce の遺伝学 |
|
- Amazon link: Pierce 2016. Genetics: A Conceptual Approach
: 使っているのは 5 版ですが、6 版を紹介しています。
Maier et al., 2005a. β-galactosidase activity as a biomarker of replicative senescence during the course of human fibroblast cultures. Ann NY Acad Sci 1100, 323–332.
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。
