脂肪細胞: 概要と目次
広告
概要: 脂肪細胞とは
脂肪細胞 adipocyte とは、細胞内に大きな油滴 lipid droplet をもつ細胞である。脂肪を蓄える役割のほか、様々なホルモンを分泌し、代謝をコントロールする機能もある。脂肪細胞を多く含む結合組織を
ヒトや マウス などの 哺乳類 には、3 種類の脂肪細胞があることが知られている (図、ref. 9)。脂肪細胞のタイプは、油滴とそれを代謝する ミトコンドリア の量比で決まる。それぞれの脂肪細胞を多く含むのが、白色、ベージュおよび褐色脂肪組織である。
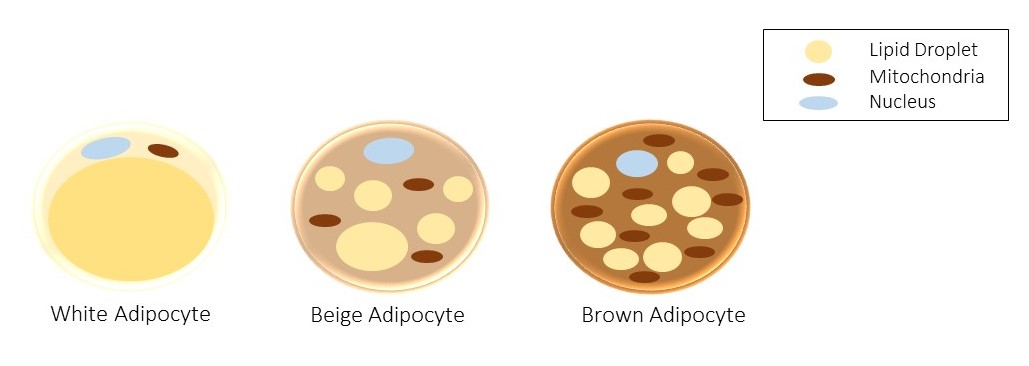
白色脂肪細胞 |
脂肪を保存するのが主な役割で、細胞質の大部分を油滴が占める。 |
ベージュ脂肪細胞 |
新しく発見されたタイプ。白色と褐色の中間。 |
褐色脂肪細胞 |
ミトコンドリアが多いため褐色を呈する。脂肪の保存ではなく、脂肪を燃焼させることで体温を維持するのが主な役割。 プロトンの濃度勾配を利用して熱を産生する UCP-1 を多く発現する。myf5-positive な細胞から分化する。myf5 は筋細胞のマーカーであり、つまり褐色脂肪細胞は細胞系譜としては筋細胞に近い。 PRDM16 は、褐色脂肪細胞特異的に発現する転写因子であり、これの発現によって myf5-positive cell が褐色脂肪細胞へ分化すると考えられている。 |
脂肪細胞の分化
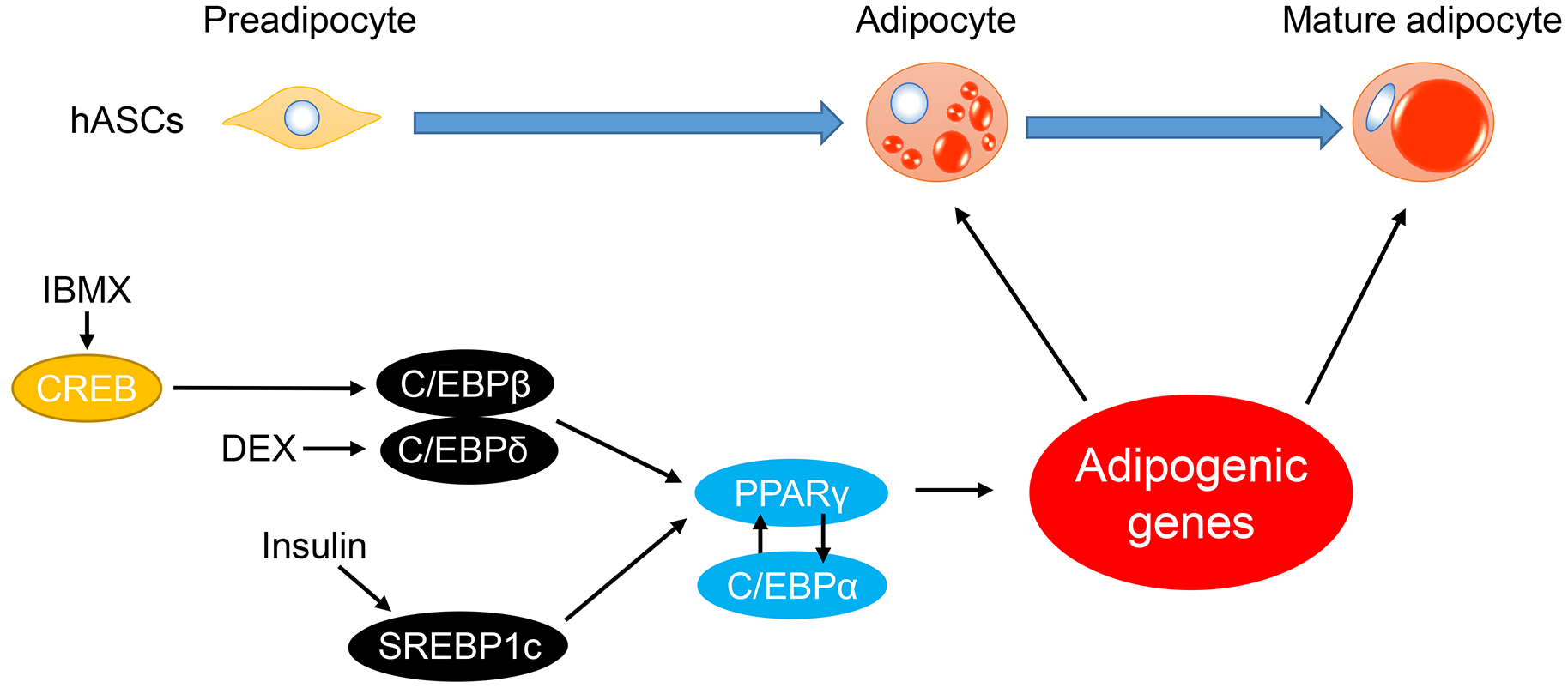
脂肪細胞は、その大きな油滴が特徴であるが、最初から油滴をもっているわけではない。図 (10) のように、前駆脂肪細胞 preadipocytes が徐々に脂肪を貯めてゆき、成熟脂肪細胞 mature adipocyte になる。この過程を脂肪細胞分化 adipocyte differentiation という。
詳細は 脂肪細胞分化 のページを参照のこと。
広告
「あとがき」で当サイトを参考にしたと書いてくれているラノベです。Kindle Unlimited で読めました。ストーリーと文章が良く、面白かったです。
脂肪細胞と肥満
肥満と診断されるには、巨大な脂肪組織が必要である。一般に、これは hyperplasia (脂肪細胞の数が増えること) と hyperprophy (脂肪細胞のサイズが大きくなること) の両方によるとされるが、一方で「脂肪細胞は分裂するのかどうか」という点が古くから問題になっていた。
> 脂肪細胞は分裂するとした日本語総説 (1)。
- 成人普通体重者の脂肪細胞は、直径 70-90 µm で、脂肪細胞の最大サイズは約 130 µm である。これは体積にして約 2.2 倍の増加。この数値をもとに考えると、BMI 約 27 までの軽度の肥満は hypertrophy で説明できるが、hyperplasia がないとそれ以上の肥満になることはできない。
- 生体脂肪組織では、前脂肪細胞の増殖が観察されないと書かれている。しかし、in vitro の系では増殖を確認しているようだ。
- 一方、成熟脂肪細胞は著者らが増殖を確認している。肥大が進み、一定のサイズに達すると増殖した。
- 肥満を肥大優勢型、肥大・増殖型、増殖型の 3 タイプに分類すること提案している。
脂肪細胞の数は、発生段階の早い時期に決定される (7) と書いてある文献もあるが、hyperplasia と hypertrophy の両方が脂肪組織のサイズに関与していることは、既にある程度のコンセンサスになっているようである。
例えば、Maumus et al. (2011, ref. 3) のイントロでは、5 つの文献を引用し、シンプルに "Excessive AT development is thought to be the result of both adipocyte hypertrophy and apparent hyperplasia" と書いてある。
さらに、最近では adipocyte dedifferentiation という、成熟脂肪細胞が脱分化して幹細胞になるプロセスも知られているようである (4)。
脂肪細胞から放出されるホルモン (アディポカイン)
脂肪細胞を多く含む結合組織である脂肪組織は、かつては単なる「余剰エネルギーの貯蔵場所」と考えられていたが、実は多くの ホルモン を放出する
以下、有名なアディポカインを表にしておく。
レプチン |
視床下部に作用して食欲を抑制する作用があり、「満腹ホルモン」などと呼ばれる。 レプチンを欠損したマウスの系統 ob/ob mice は、写真 (Public domain) のように極度の肥満を呈する。左がレプチン欠損マウス、右が野生型のマウス。 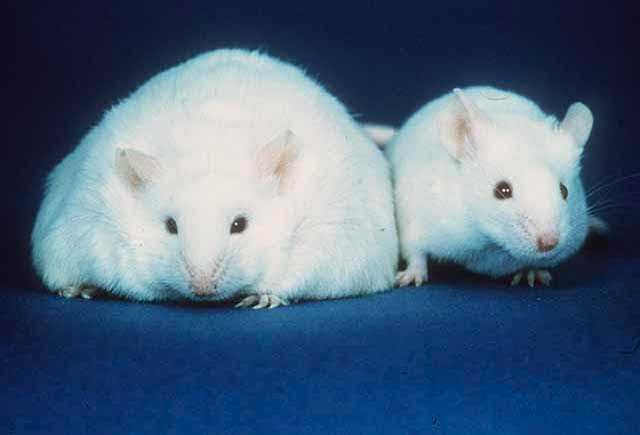
|
アディポネクチン |
インスリンの機能を増強し、血糖値を下げる働きがある。血中量が肥満の程度と逆相間することから、メタボリックシンドロームの抑制効果があるとされている。 |
油滴 lipid droplet について
油滴 lipid droplet は脂肪細胞を特徴づけるオルガネラであるが、小さい油滴は他の細胞にも存在する。詳細は 油滴 のページを参照のこと。
広告
References
杉原 2004a. 脂肪細胞の増殖. 肥満の科学.Fujimoto et al. 2008a (Review). Lipid droplets: a classic organelle with new outfits. Histochem Cell Biol 130, 263-279.Maumus et al., 2011. Native human adipose stromal cells: localization, morphology and phenotype. Int J Obesity 35, 1141-1153.Song and Kuang, 2019a (Review). Adipocyte dedifferentiation in health and diseases. Clin Sci 133, 2107-2119.- ページ分割のため削除
- ページ分割のため削除
Scioli et al. 2019a. Adipose-derived stem cells in cancer progression: new perspectives and opportunities. Int J Mol Sci 20, 3296.Schroder et al. 2019a. First insights into the effect of low-dose X-ray irradiation in adipose-derived stem cells. Int J Mol Sci 20, 6075.- By <a href="//commons.wikimedia.org/w/index.php?title=User:KTroike&action=edit&redlink=1" class="new" title="User:KTroike (page does not exist)">KTroike</a> - <span class="int-own-work" lang="en">Own work</span>, CC BY-SA 4.0, Link
Sugimoto et al., 2018a. Euglena extract suppresses adipocyte-differentiation in human adipose-derived stem cells. PLoS ONE 13, e0192404.
Figures are cited from open-access articles distributed under the terms of the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited. Also see 学術雑誌の著作権に対する姿勢.
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。
