水: 生物を構成する分子としての特徴
UBC/other_metabolites/others/water
このページの最終更新日: 2026/04/09広告
概要: 水とは
水 water は、2 個の 水素 原子と 1 個の 酸素 原子から構成される分子 H2O である。
地球上には多くの水が存在しており、生物の生育や熱の循環に重要な役割を持っている。また、水は生物の重量の 60% 以上を占める分子であり、その数%が失われただけで生命活動に影響が現れる重要な分子である。

|
|
このページは、水に関するメインページである。今のところは生化学的な内容に関する記述が多い。水に関する情報はとりあえずこのページに追加され、内容が増えてきたら独自のページに移動される。
広告
「あとがき」で当サイトを参考にしたと書いてくれているラノベです。Kindle Unlimited で読めました。ストーリーと文章が良く、面白かったです。
水分子の構造
平面構造
水分子 H2O は直線上ではなく、図 (Public domain) のように 酸素原子 を中心に折れ曲がった形をしている。水素原子の電子は酸素原子に引き寄せられており、水素は正に、酸素は負に荷電している。
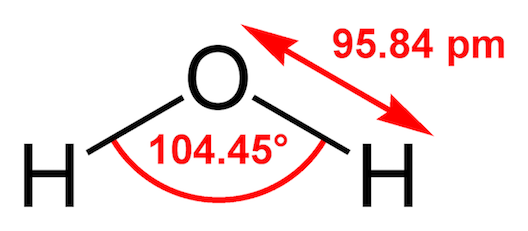
このために、水分子は電荷が非対称に分布した
3 次元構造
電子の配置を含め、水分子の構造をもう少し詳しく見てみよう。酸素原子の原子番号は 8 なので、その電子配置は次のようになる。
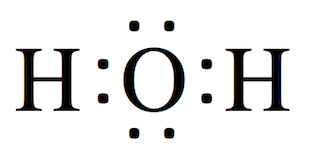
さらに詳しく見ると8 個の電子を内側から埋めていくので、1s 軌道に 2 個、2s 軌道に 2 個、2p 軌道に 4 個の電子が入る。ただし、2p 軌道の電子は 2 個がペアを組み、他の 2 個は単独で
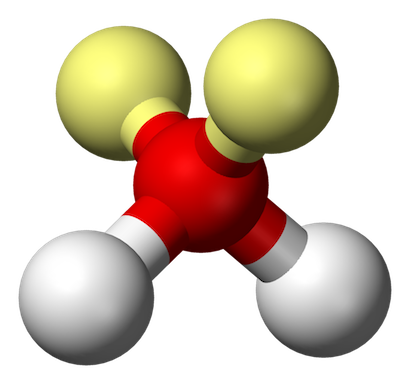
一方、水素原子は 1 個の最外殻電子をもつので、酸素原子の 2 個の不対電子と相性がよい。水の電子配置は次の図の a のようになる (図は Public domain)。
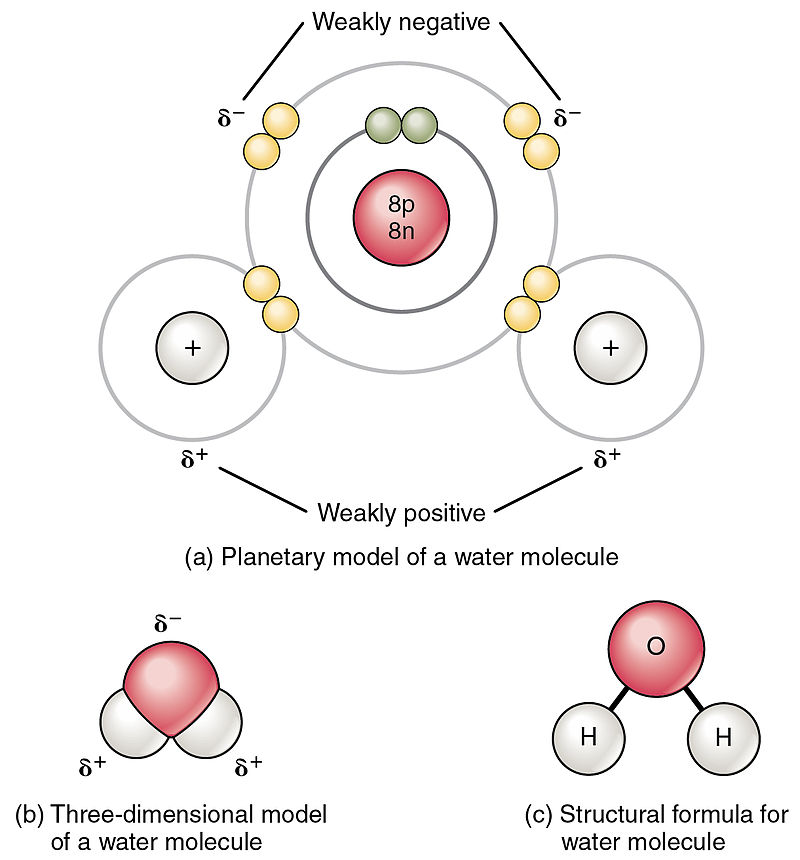
しかし水素原子が結合している分、それぞれの電子対は完全に対称ではないので、水分子は完全な四面体にはならない。結果として、水分子は図のようにわずかに歪んだ四面体としての構造をとるようになる。

|
|
アンモニア NH3 の N にも一対の電子があり、同様に四面体構造をとる。正四面体の場合は 2 つの水素原子間の角度は 109.5°になるが、水の場合は 105°、アンモニアの場合は 107° である (4)。
水素結合
水分子の特徴は、分子間で形成される多数の水素結合 hydrogen bond である (4)。これは他の溶媒に比べて著しく多く、以下のような水の特徴を生み出している。
- 多くの分子 (とくに極性のある分子) を溶かすことができる (1,3)。
- 粘性 viscosity、表面張力 surface tension、沸点 boiling point が高い。
- 凍ると体積が増える。
詳細は 水素結合のページ を参照のこと。
生体の構成要素としての水
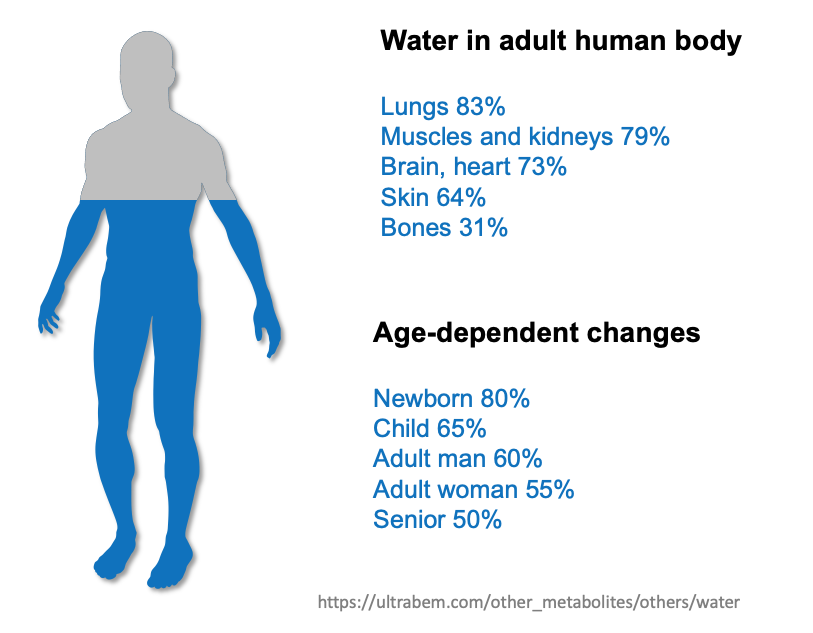
水は重量比で人体の約 60% を占め、
純水のモル濃度は 55.5 M である。
環境科学的観点からみた水
きれいな水へのアクセスは、人間の生活にとって極めて重要。食糧生産にも水は欠かせないので、水へのアクセスは 食品科学 の重要な課題の一つでもある。
その他メモ
求核試薬 nucleophile として作用できる (加水分解)。
加水分解 hydrolysis が関わる生化学イベントには、プロテアーゼ によるペプチド結合の加水分解などがある。
広告References
- Berg et al. Biochemistry: 使っているのは 6 版ですが 7 版を紹介しています。
- ページ編集に伴い削除
- ページ編集に伴い削除
- 清水 (訳) 2015a. イラストレイテッド ハーパー・生化学 30版
.
- Alberts et al. 2010a. 細胞の分子生物学
. 第 5 版.
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。
