インスリン受容体基質 IRS: 構造、機能など
UBC/protein_gene/i/irs
このページの最終更新日: 2024/02/14- 概要: IRS とは
- IRS の構造
- IRS の変異と肥満・糖尿病のリスク
広告
概要: IRS とは
インスリン受容体基質 (IRS; insulin receptor substrate) は、インスリン のシグナルを伝える分子の一つで、インスリン受容体 (IR) の次に位置する分子である。
インスリンが IR に結合すると、IR の細胞内ドメインのチロシンキナーゼが活性化し、IR を自己リン酸化する。IRS はこのリン酸化チロシンキナーゼを認識し、IR に結合する。結合後は、IR のチロシンキナーゼによって IRS のチロシンもリン酸化され、ここに複数のタンパク質が結合し、シグナルをさらに下流に伝える。
IRS の下流には、次のような分子があることが知られている。
IRS-1 は、インスリン受容体と構造の似た IGF-1 受容体にも結合する (図; ref 4)。非常に大まかに言えば、インスリンから IRS-1 を介して伝えられるシグナルは 糖質 や 脂質 の代謝を制御し (糖尿病 と関係が深い)、IGF-1 から来るシグナルは細胞分裂を制御する (がん と関係が深い)。
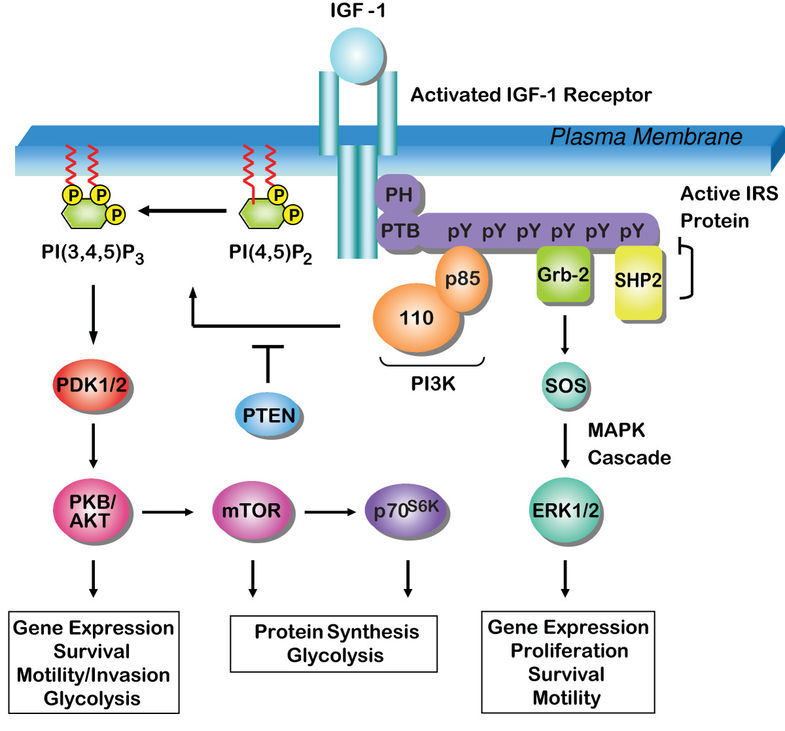
IRS の構造
N 末端側に
他の IRS アイソフォームと合わせて模式図を示す (4)。PH と PTB は IRS のドメイン、PI3K, Grb2, SHP2 は結合するタンパク質の名前。
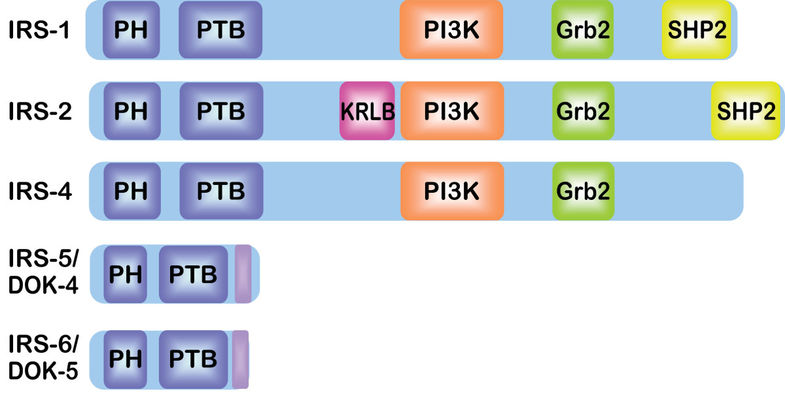
> IRS-1 に結合するタンパク質についてのレビュー (5)。
- 1985 年に発見され、のちに rat liver で初めて精製された。
- 22 の potential Tyr リン酸化サイトをもち、うち 8 個は実際にインスリンによりリン酸化されることが証明されている。
- リン酸化された Tyr が SH2 domain との binding site を形成する。
- N 末端には、SH2、SH3 ドメインなどと結合する PH domain がある。細胞膜との相互作用または IR との結合に関わっているかもしれないと書かれている。
- PH domainの隣には、PTB ドメイン。これはリン酸化した IR (NPEpY motif ) と直接結合することが yeast two-hybrid で示されている。
広告
IRS の変異と肥満・糖尿病のリスク
IRS-1
rs1801278 |
おそらく、IRS-1 で最も研究されている多型。インスリン抵抗性の原因となり、2 型糖尿病、妊娠糖尿病のリスクファクターである (1I)。チロシンリン酸化領域に存在し、PI-3 kinase との結合に影響すると考えられる (1I)。
|
rs1864010 |
プロモーター領域の SNP で、Sp1-binding site にある (SNPedia)。Colorectal cancer と相関している。 |
rs1801278 |
G → A の変異が メタボリックシンドローム のリスクと相関している。特に喫煙者で → PubMed. |
rs2943641 |
2011 年に報告された多型。日本人を対象にした研究。→ Paper link. |
IRS-2
IRS-2 |
IRS-2 の G1057D 変異。DD genotype は GG genotype よりも妊娠糖尿病のリスクが高い (2) |
広告
References
Alharbi et al. 2014a. Insulin receptor substrate-1 (IRS-1) Gly927Arg: correlation with gestational diabetes mellitus in Saudi women. BioMed Res Int 146495.Ayaz et al. 2014a. The G1057D polymorphism of insulin receptor substrate-2 associated with gestational diabetes mellitus. Gynecol Endocrinol 30, 165-168.Fallucca et al. 2006a. Polymorphisms iof insulin receprot substrate 1 and β3-adrenergic receptor genes in gestational diabetes and normal pregnancy. Metab Clin Exp 55, 1451-1456.Mardilovich et al. 2009a. Expression and function of the insulin receptor substrate proteins in cancer. Cell Commn Signaling 7, 14.Ogawa et al. 1998a. Role of binding proteins to IRS-1 in insulin signaling. Mol Cell Biochem 182, 13-22.
Mardilovich et al. 2009a. is an open-access article distributed under the terms of the Creative Commons Attribution License, which permits unrestricted use, distribution, and reproduction in any medium, provided the original author and source are credited. Also see 学術雑誌の著作権に対する姿勢.
コメント欄
サーバー移転のため、コメント欄は一時閉鎖中です。サイドバーから「管理人への質問」へどうぞ。
